Salz, das weiße Gold, ist einerseits für uns Menschen lebenswichtig, andererseits kann es uns aber in zu großen Mengen auch krank machen. Was für uns jedoch zu viel ist, ist für bestimmte Mikroorganismen aber gerade richtig, um existieren zu können. Verrückte Welt!
In so ziemlich jedem Haushalt befindet sich Kochsalz (NaCl). Es enthält wichtige Elektrolyte (Na+ und Cl–), die wir zum Überleben brauchen, da sie im Körper bestimmte Funktionen erfüllen. Sogar einer unserer Geschmackssinne ist allein für das schmecken von Salz reserviert.
Allerdings hat Salz nicht nur gute Seiten. Es kann auch gefährlich werden! Denn Salz in unserem Blut zieht Wasser an, wodurch sich das Flüssigkeitsvolumen in den Gefäßen erhöht und somit der Blutdruck steigt. Das Schlaganfallrisiko wird begünstigt! Laut des Britisch Medical Journal sterben weltweit 1,65 Millionen Menschen pro Jahr an überhöhtem Salzkonsum.
Wie viel Salz darf es sein?
Ein erwachsener Mensch benötigt circa 5-6 Gramm Salz pro Tag. Wiegen Sie einfach mal auf einer Küchenwage diese Menge ab. Sie werden überrascht sein, wie wenig das eigentlich ist! Vor allem versteckte Salzmengen, wie zum Beispiel in Schokolade oder total überwürzten Fertiggerichten machen uns das Leben schwer und die Kontrolle der Salzmenge schier unmöglich.
Aber es gibt auch Lebewesen, die besonders hohe Salzkonzentrationen in ihrer Umgebung bis hin zur Sättigung vertragen und diese auch zum Wachstum und Leben brauchen. Diese werden als extrem halophile (= „Salz liebende“) Organismen bezeichnet. Besondere Vertreter sind hier die Halobakterien, die zur Gruppe der Archaeen gehören. Archaeen unterscheiden sich von Bakterien zum Beispiel im Aufbau der Zellwand und der Resistenz gegenüber Antibiotika. Die Halobakterien bevorzugen Salzkonzentrationen von 32 Prozent, welches einer gesättigten Kochsalzlösung entspricht. Respekt! Daher ist es nicht verwunderlich, dass sie sich zum Beispiel in Salzseen oder Salinen besonders wohl fühlen.
Wie machen die das?
Wie bereits oben erwähnt, zieht Salz Wasser an. Das heißt, ist die Salzkonzentration außerhalb des Organismus höher als in seinem Inneren, wie es im Lebensraum Halophiler üblicherweise der Fall ist, dann würde dem Organismus Wasser entzogen, sprich, er würde austrocknen. Diesen Effekt nennt man Osmose:
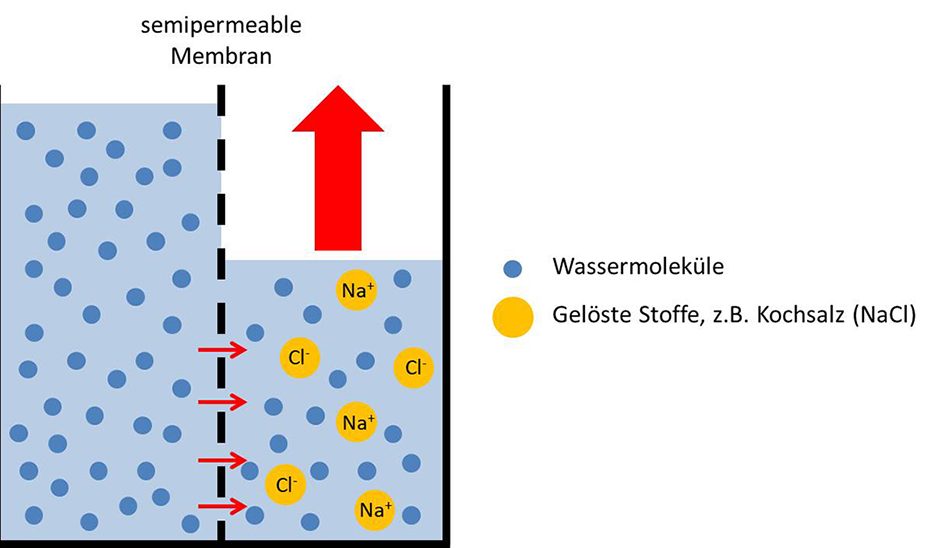
Wasser diffundiert vom Bereich mit hoher Wasserkonzentration (niedrige Konzentration gelöster Stoffe) zum Bereich mit geringer Wasserkonzentration (hohe Konzentration gelöster Stoffe) durch eine halbdurchlässige (semipermeable) Membran. Diese Membran zeichnet sich dadurch aus, dass sie nur für bestimmte Stoffe durchlässig ist. Das heißt, dass das Wasser immer durch die Membran wandern kann, aber nicht die gelösten Stoffe, z.B. Salze. Das Ziel der Osmose ist der Konzentrationsausgleich auf beiden Seiten der Membran!

Gegen diesen osmotischen Effekt sind die Halobakterien jedoch gefeit. Beispielsweise Halobacterium, der bestuntersuchteste Vertreter der Halobakterien, pumpt Kalium-Ionen (K+) in großen Mengen aus der Umgebung in sein Zellinneres, wodurch die K+-Konzentration hier viel höher ist als die Na+-Konzentration außerhalb der Zelle. Kurz gesagt, die Konzentration an gelösten Stoffen innerhalb der Zelle wird größer als außen, die Wasserkonzentration im Zellinneren somit geringer und das Diffundieren von Wasser aus der Zelle verhindert.
Die K+-Ionen wirken bei Halobacterium als Osmoprotektant. Osmoprotektanzien sind Substanzen, die von den Mikroorganismen selbst hergestellt oder aus der Umwelt aufgenommen und im Zellinneren angereichert werden, um eine positive Wasserbalance aufrecht zu erhalten. Diese Substanzen dürfen die biochemischen Prozesse in der Zelle aber nicht hemmen. Beispiele hierfür sind stark wasserlösliche Zucker, Aminosäuren oder Zuckeralkohole.
Um den Effekt der Osmose zu veranschaulichen, möchten wir Sie gerne auf folgendes Experiment aufmerksam machen:
https://www.phywe.de/de/osmose-abhaengigkeit-des-osmotischen-drucks-von-der-konzentration.html